肝臓のティッシュエンジニアリング
須藤 亮,谷下 一夫(慶応義塾大学)
理工学と生物・医学との学際領域である生体工学の分野では,既存の理工学や生物・医学における知識を応用することで新しい概念や研究成果が生まれることが期待されている.近年,特定の学問分野が掘り下げられて研究されている一方で,それぞれの学問分野の境界を取り払い,お互いをうまく統合させることによって新しいシステムパラダイムを模索する方向性が示されてきた.特に,20世紀型の科学技術に対する新しいシステムパラダイムとして生命システムのもつ特性を人工システムに応用する概念が注目されている[1].全体の統合性が巧妙に保たれている生命システムの原理を工学的に理解することが可能になれば,生命とは無関係な他の人工システムに応用することが可能となり,画期的なシステムの制御方法などが開発されるものと思われる.
生命システムは,自己組織性,階層性,自己修復性など,いずれも従来の人工システムには取り入れられていない巧みな特徴を有している.私たち人の体を1つのシステムとして考えると,このような生命システムを構成しているのは,肝臓・腎臓・心臓などのような臓器や,血管・筋肉・骨などの組織であり,これらのサブシステムが個別に機能していると同時にそれぞれの間には相互作用があることで全体として協調している.さらにミクロな視点で考えてみると,それぞれの臓器を構成している細胞が最も単純な機能を担っている要素であることが分かる.生命システムの要素である細胞は,単なる集合体を形成するだけでなく有機的に組み合わさることで組織となり,全体が要素の総和以上のものとして新しい機能を獲得している.このように組織としての機能を獲得するメカニズムには不明な点が多く,工学的な理解も進んでいない.したがって,細胞がいかにして生命として機能しているかという点について解明することは生命システムの原理を工学的に理解するための重要な課題である.
肝臓は人体の中でも最大の臓器であり,生命システムにおいて特徴的な自己修復性をもつ.たとえば,ラットの肝臓を70%切除した場合でも,肝臓の組織は非常に複雑であるにもかかわらず2週間もすると残存した肝臓が元通りの大きさになるまで再生する.また,ヒトの場合においても肝移植が可能であることから同様の再生能力をもつことがわかる.このような肝臓の細胞がもつ自己組織性,自己修復性を生体外で再現させることは生命システムの原理を工学的に理解するために重要なアプローチとなる.しかし,生体内で旺盛な再生能力をもつ肝細胞も生体外に分離して培養系に移すと急激にその能力を失ってしまい,最終的に死滅してしまう.このように通常の肝細胞では生体外で機能を維持することができなかったが,近年の研究成果によって幹細胞あるいは前駆細胞と呼ばれる特殊な細胞を特異的に分離してくることによって生体外でも組織を再生できる可能性が示されてきた.たとえば,ES細胞(Embryonic Stem Cell: 胚性幹細胞)は万能細胞とも呼ばれ,体中のあらゆる組織になりうる能力をもつ.また,骨髄中にも同様の多能性を持つ細胞が存在することが報告されている.さらに,肝臓においても小型肝細胞と呼ばれる増殖能力をもつ細胞が存在し,この細胞を特異的に分離してくることで生体外においても肝臓に類似した組織を再現させることが可能になってきた[2].
当研究室においても小型肝細胞のもつ自己組織性に着目して研究を進めてきた.その結果,ラットの肝臓から小型肝細胞を分離して培養することで生体外に毛細胆管を再形成させることに成功した[3].毛細胆管とは,隣接する肝細胞の境界に形成されている直径1マイクロメートルほどの管構造であり,肝細胞から分泌された胆汁成分や代謝産物の通り道になっている.分離直後の小型肝細胞を顕微鏡で観察すると,ばらばらの状態で無秩序に配置されており,生体内で形成していた毛細胆管は失われている.しかし,培養するに従って細胞が増殖するだけでなく,その配列にも徐々に秩序が生まれて一定の構造を再生し,最終的には毛細胆管までもが再生された(図1).再生した毛細胆管は,生体内と同様の機能を持ち,収縮,拡張を繰り返していることが分かった.さらに,ネットワーク状に成長した毛細胆管は,それぞれの部分がランダムに運動するのではなく,ネットワーク全体で同期して収縮運動を行うことにより内容物を輸送するポンプとしての機能を有することが明らかになった[4].すなわち,毛細胆管ネットワークを形成している一連の小型肝細胞は,個別にふるまうのではなく集団としてまとまったふるまいをすることで組織としての機能を獲得したことを意味している.この結果は,まさに肝細胞の自己組織性,自己修復性といった特徴を端的に表した現象であると言える.
このような細胞の自己組織性を利用して組織を再生させる技術は再生医療への応用が考えられる.たとえば,肝細胞から肝組織を再生させることができれば,肝移植に代わる治療法として細胞組織移植が考えられ,肝移植におけるドナー不足の問題を解消できるかもしれない.そこで,従来の研究では細胞を二次元で培養していたのに対し,実際の組織は三次元の複雑な構造をもつことから,最近は「いかにして三次元組織を再生させるか?」ということがティッシュエンジニアリングにおける重要な課題になっている.また,組織を三次元で成長させるためには,組織表面からの拡散だけでは酸素や栄養の供給が不十分である.このような問題に対してこれまでの研究成果に加えて,マイクロレベルでの熱物質移動など熱工学における知識も応用することで三次元構造を有する複雑な組織を再生させることを目指していきたい.
【参考文献】
[1] 日本機械学会編,メカノクリーチャ,コロナ社,2003
[2] 三高 俊広,肝臓における幹細胞システムと肝組織再構築,実験医学,18 (4), 431–437, 2000.
[3] Sudo et al., Bile canalicular formation in hepatic organoid reconstructed by rat small hepatocytes and nonparenchymal cells. J Cell Physiol. 199 (2): 252–261, 2004.
[4] Sudo et al., Coordinated movement of bile canalicular networks reconstructed by rat small hepatocytes. Ann Biomed Eng. In press.
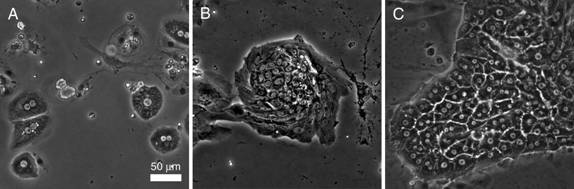
図1 小型肝細胞の自己組織化を示す位相差顕微鏡写真.(A) ラットの肝臓から分離した培養1日目の細胞.各細胞がランダムに配置されている.(B) 培養10日目.小型肝細胞が増殖することで集合体を形成する.(C) 培養20日目.小型肝細胞の集合体において形態形成が起こり,肝組織に類似した構造が再形成されてくる.図において白く筋状に見える部分が毛細胆管である.